Aktualizacja: 6 maja 2026
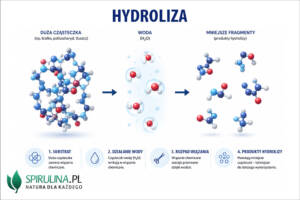 Hydroliza to powszechny proces chemiczny, w przebiegu którego pod wpływem wody dany związek chemiczny ulega rozpadowi na mniejsze fragmenty. Innymi słowy, działanie wody rozbija organiczny związek chemiczny, czego efektem jest powstanie nowych związków. Bywa to szeroko wykorzystywane w różnych dziedzinach przemysłu i życia.
Hydroliza to powszechny proces chemiczny, w przebiegu którego pod wpływem wody dany związek chemiczny ulega rozpadowi na mniejsze fragmenty. Innymi słowy, działanie wody rozbija organiczny związek chemiczny, czego efektem jest powstanie nowych związków. Bywa to szeroko wykorzystywane w różnych dziedzinach przemysłu i życia.
Na czym polega hydroliza?
Hydroliza jest procesem zachodzącym w trakcie rozpuszczania w wodzie soli mających w swoim składzie kation pochodzący od słabej zasady i/lub anion pochodzący od słabego kwasu. Słabe kwasy i zasady hydrolizie nie ulegają. W przypadku hydrolizy kationu słabej zasady mamy do czynienia z hydrolizą kationową, z kolei w przypadku hydrolizy anionu słabego kwasu, z hydrolizą anionową. Konsekwencją hydrolizy jest odpowiednio kwasowe lub zasadowe pH roztworu wodnego. Omawiając to od nieco innej strony można powiedzieć, że hydroliza polega na rozkładzie związku chemicznego z udziałem wody. Cząsteczka zostaje „rozcięta” na mniejsze fragmenty, a woda dostarcza do tego procesu swoje składniki: wodór (H) i grupę hydroksylową (OH).
Należy podkreślać, że reakcjom hydrolizy nie ulegają sole mocnych zasad i mocnych kwasów, takie jak:
- NaCl;
- Na2SO4;
- KNO3;
- CaCl2;
- KClO4.
Reakcjom hydrolizy ulegają natomiast:
- sole mocnych zasad i słabych kwasów, np. CH3COONa, NaCN, KNO2, HCOOK, Na2CO3, Na2S – hydroliza zasadowa;
- sole słabych zasad i mocnych kwasów, np. NH4Cl, AlCl3, Zn(NO3)2, FeBr3, CuCl2, NiSO4 – hydroliza kwasowa;
- sole słabych zasad i słabych kwasów, np. NH4NO2, CH3COONH4, (HCOO)3Al – hydroliza kwasowo-zasadowa.
Procesy te zachodzą powszechnie wokół nas, w środowisku naturalnym i w gospodarstwach domowych. Są też świadomie wykorzystywane w produkcji różnorodnych roztworów i produktów na skalę przemysłową.
Hydroliza – przykłady
W życiu codziennym klasycznym przykładem hydrolizy jest produkcja mydła, a więc hydroliza tłuszczów w reakcji z zasadą, co prowadzi do efektu zmydlania. Innym przykładem może być rozkład detergentów w wodzie podczas domowych obowiązków i sprzątania. Reakcjom hydrolizy podlegają ponadto białka w układzie pokarmowym człowieka, czego efektem jest rozłożenie długich łańcuchów białkowych na mniejsze cząsteczki nazywane aminokwasami, jak również trawienie tłuszczów, czego efektem będzie powstanie kwasów tłuszczowych i glicerolu w środowisku hydrolizy. W chemii wykorzystuje się fakt, że niektóre sole reagują z wodą, zmieniając pH roztworu. W przyrodzie przykładem hydrolizy może być rozkład materii organicznej w glebie.
Proste przykłady chemiczne:
- sacharoza (cukier stołowy) ulega hydrolizie w środowisku wodnym, rozpuszczając się i dając glukozę + fruktozę;
- laktoza (cukier mleczny) ulega hydrolizie na etapie produkcji mleka bezlaktozowego, dając glukozę + galaktozę.
Takich przykładów jest oczywiście znacznie więcej, dlatego z pewnością warto wiedzieć, czym jest hydroliza.

 Spirulina w tabletkach (100% naturalna)
Spirulina w tabletkach (100% naturalna)Spirulina posiada w pełni naturalne witaminy i minerały o wysokim stężeniu. W jej skład wchodzą m.in.: biotyna, beta-karoten, kwas foliowy, tiamina, niacyna, witamina D, E i inne witaminy oraz białko i błonnik. To też źródło cynku, magnezu, wapnia, żelaza
Zobacz tutaj ...
 Spirulina w proszku (100% naturalna)
Spirulina w proszku (100% naturalna)Spirulina w proszku to słodkowodna alga, zawierająca duże stężenie witamin, minerałów i innych, ważnych składników odżywczych. Wysoką jakość uzyskano dzięki odpowiednim warunkom klimatycznym, przestrzeganiu restrykcyjnych norm podczas hodowli i …
Zobacz tutaj ...
Bibliografia
- Łazarenkow A., Ćwiczenia laboratoryjne z przedmiotu nauczania: „Chemia Ogólna i Nieorganiczna” dla studentów I roku Kierunku Farmacja, Łódź 2022.
- McMurry J., Chemia organiczna, Wydawnictwo PWN, Warszawa 2017.






Zostaw komentarz